هندسة عقلانية تُنتج أداة مدمجة جديدة لعلاج الجينات
مقدمة
أعلن باحثون من معهد ماكغفرن لأبحاث الدماغ في معهد ماساتشوستس للتكنولوجيا ومعهد براود التابع لمعهد ماساتشوستس للتكنولوجيا وجامعة هارفارد عن تطويرهم لإنزيم RNA-guided مضغوط مُهندس وراثيًا، يُعدّ أداة فعّالة وقابلة للبرمجة لتحرير الجينوم البشري. يُسمى هذا البروتين NovaIscB، وهو قادر على إجراء تعديلات دقيقة على الشفرة الوراثية، وتعديل نشاط جينات محددة، بالإضافة إلى مهام تحرير أخرى. وبسبب صغر حجمه، الذي يُسهّل وصوله إلى الخلايا، يُعتبر NovaIscB مرشحًا واعدًا لتطوير علاجات جينية لمعالجة الأمراض أو الوقاية منها. وقد نُشرت هذه الدراسة التي قادها البروفيسور فنغ زانغ، أستاذ علم الأعصاب في معهد ماساتشوستس للتكنولوجيا وباحث في معهد ماكغفرن ومعهد هوارد هيوز الطبي، وعضو أساسي في معهد براود، في مجلة Nature Biotechnology.
أصل NovaIscB وخصائصه
يُشتق NovaIscB من قاطع DNA بكتيري ينتمي إلى عائلة من البروتينات تسمى IscBs، والتي اكتشفها مختبر زانغ في عام 2021. تُعدّ IscBs نوعًا من أنظمة OMEGA، وهي أسلاف Cas9 التطورية، وهي جزء من نظام CRISPR البكتيري الذي طوره زانغ وآخرون إلى أدوات قوية لتحرير الجينوم. مثل Cas9، تقطع إنزيمات IscB الـ DNA في مواقع محددة بواسطة دليل RNA. من خلال إعادة برمجة هذا الدليل، يمكن للباحثين إعادة توجيه الإنزيمات إلى تسلسلات اختيارية.
لفتت IscBs انتباه الفريق ليس فقط لأنها تشترك في سمات رئيسية مع Cas9 القاطع للـ DNA في CRISPR، ولكن أيضًا لأن حجمها يمثل ثلث حجم Cas9. وهذه ميزة كبيرة للعلاجات الجينية المحتملة؛ حيث إن الأدوات المدمجة أسهل في توصيلها إلى الخلايا، ومع إنزيم صغير، سيكون لدى الباحثين مرونة أكبر للتلاعب به، وإضافة وظائف جديدة دون إنشاء أدوات كبيرة جدًا للاستخدام السريري.
عملية الهندسة العقلانية لـ NovaIscB
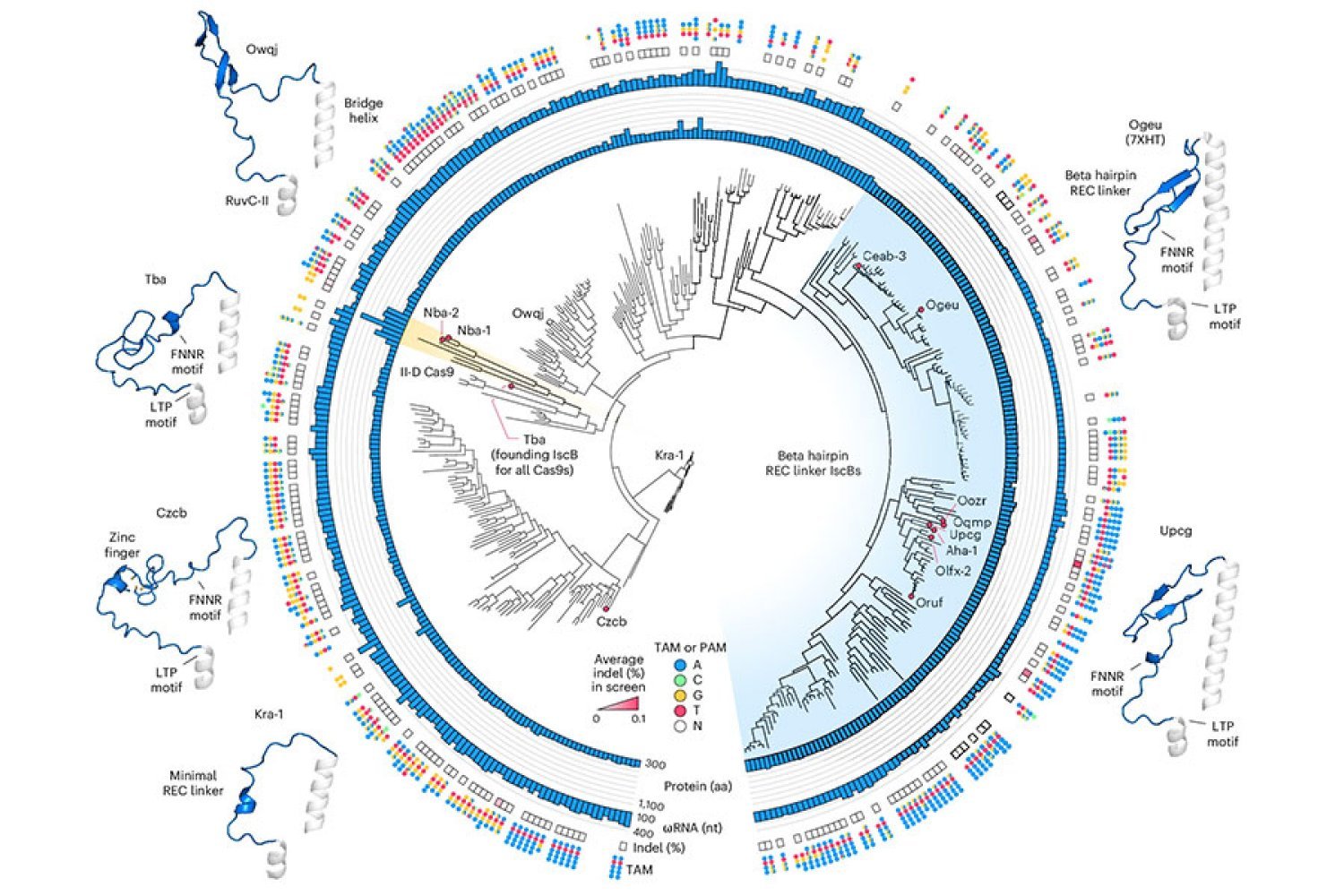
في البداية، قام الباحثون بفحص ما يقرب من 400 إنزيم IscB مختلف وجدوا في البكتيريا، واختاروا عشرة منها قادرة على تحرير DNA في الخلايا البشرية. لكن حتى أكثرها نشاطًا احتاج إلى تحسين ليصبح أداة تحرير جينوم مفيدة. كان التحدي هو زيادة نشاط الإنزيم، ولكن فقط في التسلسلات المحددة بواسطة دليل RNA الخاص به. إذا أصبح الإنزيم أكثر نشاطًا بشكل عشوائي، فسيقطع الـ DNA في أماكن غير مرغوب فيها.
ركز الباحثون على إطالة دليل RNA، مما يقلل من احتمالية عمل IscB على تسلسلات خارج الهدف المحدد. استخدموا المعلومات المتعلقة بتنوع IscBs البكتيرية وكيفية تطورها، ولاحظوا أن IscBs التي تعمل في الخلايا البشرية تتضمن مقطعًا يسمى REC، والذي كان غائبًا في IscBs الأخرى. أظهر النمذجة البنيوية أن توسيع جزء من البروتين REC قد يُمكّن IscBs من التعرف على أدلة RNA أطول.
قام الفريق بتجربة تبديل أجزاء من مجالات REC من IscBs و Cas9s مختلفة، وتقييم تأثير كل تغيير على وظيفة البروتين. باستخدام فهمهم لكيفية تفاعل IscBs و Cas9s مع كل من DNA وأدلة RNA الخاصة بهم، قاموا بإجراء تغييرات إضافية بهدف تحسين كفاءة ونوعية التحرير. نتج عن ذلك بروتين NovaIscB، الذي كان أكثر نشاطًا في الخلايا البشرية بأكثر من 100 مرة من IscB الأصلي، وقد أظهر خصوصية جيدة لأهدافه. وقد استخدموا أداة الذكاء الاصطناعي AlphaFold2 للتنبؤ بكيفية تأثير كل تعديل على بنية البروتين.
تطبيقات NovaIscB و آفاق المستقبل
أظهر الفريق أن NovaIscB هو هيكل جيد لمجموعة متنوعة من أدوات تحرير الجينوم. استخدموا NovaIscB لاستبدال أحرف محددة من شفرة DNA في الخلايا البشرية، وتغيير نشاط الجينات المستهدفة. كما تم استخدام NovaIscB في إنشاء أداة تسمى OMEGAoff، والتي تضيف علامات كيميائية إلى DNA لتقليل نشاط جينات محددة. وقد تم استخدامها بنجاح في خفض مستويات الكوليسترول في فئران التجارب.
يُعدّ حجم NovaIscB الصغير ميزة كبيرة، حيث يمكن تغليفه بسهولة داخل فيروس معدي مرتبط بالغدة (AAV)، وهو الناقل الأكثر استخدامًا لتوصيل العلاج الجيني بأمان للمرضى. يُتوقع أن يُستخدم NovaIscB لاستهداف أدوات تحرير الجينوم لمعظم الجينات البشرية، ويتطلع الفريق لرؤية كيفية استخدام المختبرات الأخرى لهذه التقنية الجديدة. كما يأملون في أن يتبنى الآخرون نهجهم في الهندسة العقلانية للبروتينات.









اترك تعليقاً